Les
sals
Les sals són compostos iònics que es formen per la unió d'un catió metàl·lic amb un anió que pot ser:
-
Derivat dels hidràcids (F-, Cl-,...)
-
Derivat dels oxoàcids (ClO-, SO42-,...)
- Són combinacions
binàries d'un catió metàl·lic
amb els anions resultants de la dissociació dels hidràcids
que, recordem, s'anomenen amb la terminació -ur:
- F- ió fluorur
- Cl- ió clorur
- Br- ió bromur
- I- ió iodur
- S2- ió sulfur
- Se2- ió selenur
- Te2- ió tel·lurur
- No contenen oxigen.
- Formulació: METALL + NO METALL. Cal
combinar els cations i els anions de manera que la càrrega final
sigui zero.
- Per formular la sal que es formaria entre el catió Fe3+ i l'anió Br-, hem de tenir en compte que necessitarem tres anions bromur per anul·lar les tres càrregues del catió ferro (III): FeBr3.
- Nomenclatura: s'anomenen arrel del nom del no metall -ur de nom metall. Si el metall pot tenir més d'un estat d'oxidació, cal especificar-lo entre parèntesi i amb xifres romanes.
- Exemple: NaBr, bromur de sodi.
Sals derivades dels oxoàcids
- Són combinacions ternàries d'un catió metàl·lic amb els anions resultants de la dissociació dels oxoàcids.
- Recordem que:
- Quan estan en dissolució aquosa, els oxoàcids perden els hidrògens en forma d'ions H+.
- L'anió que es forma és poliatòmic, és a dir, està format per dos o més àtoms units de manera covalent.
- Els anions resultants s'anomenen amb
les terminacions:
- -it si l'àcid acabava en -ós.
- -at si l'àcid acabava en -ic.
- Si els àcids tenien el prefix hipo- o per-, els anions el conserven.
Els anions derivats dels oxoàcids
|
Oxoàcid
|
Nom
oxoàcid
|
Anió
|
Nom
anió
|
| HClO | Àcid hipoclorós | ClO- | Anió hipoclorit |
| HClO2 | Àcid clorós | ClO2- | Anió clorat |
| HClO3 | Àcid clòric | ClO3- | Anió clorat |
| HClO4 | Àcid perclòric | ClO4- | Anió perclorat |
| HBrO | Àcid hipobromós | BrO- | Anió hipobromit |
| HBrO2 | Àcid bromós | BrO2- | Anió bromit |
| HBrO3 | Àcid bròmic | BrO3- | Anió bromat |
| HBrO4 | Àcid perbròmic | BrO4- | Anió perbromat |
| HIO | Àcid hipoiodós | IO- | Anió hipoiodit |
| HIO3 | Àcid iòdic | IO3- | Anió iodat |
| HIO4 | Àcid periòdic | IO4- | Anió periodat |
| HMnO4 | Àcid permangànic | MnO4- | Anió permanganat |
| H2SO3 | Àcid sulfurós | SO32- | Anió sulfit |
| H2SO4 | Àcid sulfúric | SO42- | Anió sulfat |
| HNO2 | Àcid nitrós | NO2- | Anió nitrit |
| HNO3 | Àcid nítric | NO3- | Anió nitrat |
| H3PO4 | Àcid fosfòric | PO43- | Anió fosfat |
| H2CO3 | Àcid carbònic | CO32- | Anió carbonat |
- Formulació: METALL + OXOANIÓ.
Cal combinar els cations i els anions de manera que la càrrega
final sigui zero.
- Per formular la sal que es formaria entre el catió Fe3+ i l'anió BrO-, hem de tenir en compte que necessitarem tres anions bromur per anul·lar les tres càrregues del catió ferro (III): FeBrO3.
- Si hem de combinar més d'un anió l'hem d'escriure entre parèntesi amb el subíndex corresponent.
- Nomenclatura: s'anomenen nom de l'anió de nom metall. Si el metall pot tenir més d'un estat d'oxidació, cal especificar-lo entre parèntesi i amb xifres romanes.
- Exemple: NaBrO, hipobromit de sodi; Ca(BrO)2, hipobromit de calci.
Més informació:
http://www.iesberenguer.net/departaments/fisicaiquimica/inorganica/apuntsino1.htm

La formació de l'hipoclorit de sodi a partir del catió sodi i l'anió hipoclorit
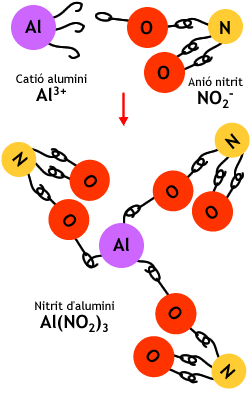
La formació del nitrit d'alumini a partir del catió alumini i l'anió nitrit
![]() Material elaborat per Irene Martínez
Material elaborat per Irene Martínez
![]()

Aquesta obra està subjecta a una Llicència
de Creative Commons.