|
| Començar | Galeria
de Fotos | Glossari | Jocs
| Pedagogia |
Problemes
| Sortir |
|

|
| Aquí teniu unes quantes adreces on hi ha indicats alguns experiments
de química que es poden fer amb els elements que es tenen a la cuina.
Com sempre, tenen la pega d'estar en anglès, així que n'hem
traduït tres per a que en tingueu una mostra. Si
proveu de fer-los, no canvieu cap dels ingredients i proporcions, i sobre
tot: un adult que supervisi el que feu ! |
|
| Adreces d'internet |
|
Segur que vosaltres podreu trobar altres llocs tant interessants o més
que aquests! |
|
| Experiments
per fer a casa: traduccions |
|
|
|
| Construeix
el teu propi volcà |
 |
|
| Construirem un volcà que expulsarà lava vermella per
les seves vessants. |
| Materials |
-
Sal de cuina
-
farina
-
oli
-
aigua
-
llevat del tipus "Royal"
-
Colorant d'alimentació vermell
-
detergent líquid
-
vinagre
|
-
una ampolla de plàstic
-
1 bol gran
-
1 tassa d'esmorzar
-
1 cullera sopera
-
1 cassola
|
|
| Procediment |
-
En un bol gran barregem 6 tasses de farina, 2 tasses de sal, 4 cullerades
d'oli i 2 tasses d'aigua. Treballem els ingredients amb les mans fins que
la massa agafi una consistència suau i ferma. Si es necessita es
pot afegir una mica més d'aigua.
-
Col·loquem l'ampolla dins de la cassola. Posem la pasta al voltant
de l'ampolla, amb molt de compte de no tapar la boca de l'ampolla
ni de que caigui gens de pasta a dins. Hem d'anar amb molta cura en aquest
pas, prenen tot el temps que ens calgui. Podem donar forma a tants
detalls com voguem al nostre volcà.
-
Omplim l'ampolla gairebé fins a dalt amb aigua tèbia barrejada
amb el colorant alimentari.
-
Posem 6 gotes de detergent líquid dins l'ampolla
-
Afegim 2 cullerades de llevat.
-
A poc a poc afegim vinagre dins l'ampolla i ens apartem ràpidament.
|
| Discussió |
| Veurem com comença a sortir lava vermella del volcà.
Això és degut a que la reacció del llevat amb el vinagre,
que produeix diòxid de carboni (CO2), el mateix gas que
es forma en els volcans de veritat. Les bombolles de gas que es formen
forcen la "lava" líquida de l'ampolla a sortir i baixar per les
vessants del volcà. |
| (Font: el laboratori
del Dr. Reeko) |
|
| Test
del midó |
 |
|
| materials |
-
tassa d'esmorzar
-
farina
-
tintura de iode (el "topionic" també pot servir).
-
mostres de pernil dolç de diversos preus.
|
| Procediment |
-
posa una mica de farina a la tassa.
-
deixa caure algunes gotes de tintura de iode a la farina.
-
fes el mateix en cadascuna de les mostres de pernil.
|
| NO MENGEU LA FARINA QUE S'HA FET SERVIR EN AQUEST
EXPERIMENT. EL IODE ÉS VERINÓS!!! |
|
| Discussió |
| En química, moltes substàncies canvien de color degut
a reaccions amb d'altres substàncies. Un exemple d'això n'és
el iode. El iode es torna blau sempre que reacciona amb el midó.
Això vol dir que és un indicador molt útil per detectar
midó, simplement deixant caure algunes gotes de iode en una mostra.
En aquest cas hem triat el pernil dolç. |
|
| Si el pernil dolç fos simplement la cuixa o l'espatlla
del porc bullit i prou, NO HAURIA DE REACCIONAR AMB EL MIDÓ,
ja que el midó és una proteïna d'origen vegetal.
Si el pernil dolç ha estat adulterat, és a dir, se li ha
afegit patata o d'altres materials farinosos en la seva elaboració
llavors aquest pernil reaccionarà amb el iode. |
|
| NO MENGEU EL PERNIL QUE S'HA FET SERVIR EN AQUEST
EXPERIMENT. EL IODE ÉS VERINÓS!!! |
|
| Font: aquesta la saben tots els professors del món i part de
l'estranger....J |
|
| Neteja
de l'argent sense líquids comercials |
 |
|
| Si teniu objectes fets amb argent o argentats, sabreu que la superfície
lluent d'aquests es va ennegrint i perden la lluentor. Això ocorre
perquè l'argent pateix una reacció amb les substàncies
de l'aire que contenen sofre. Podeu fer servir la química per invertir
la reacció. |
|
materials
|
-
Una peça d'argent ennegrit.
-
Aigua
-
Llevat del tipus "Royal", aproximadament 1 tassa per cada 4 litres d'aigua.
-
Full d'alumini.
|
-
Una cassola o un plat prou gran com per tenir completament submergit l'argent
en el fons de la cassola o plat.
-
recipient per escalfar l'aigua.
-
guants de cuina.
|
|
| Procediment |
| Recobrim el fons de la cassola amb el full d'alumini. Col·loquem
la peça d'argent sobre l'alumini, assegurant-nos bé
que l'argent el toqui. |
|
| Escalfem l'aigua fins que bulli. L'enretirem del foc (amb els guants
de cuina) i la posem dins de la pica (posem alguna cosa, com un protector
de plàstic o una tovallola entre la pica i el recipient per a que
la calor no trenqui la pica). Afegim el llevat necessari a l'aigua. La
barreja pot esquitxar i bombollejar una mica, és per això
que la posem a la pica. |
|
| Gairebé immediatament l'ennegriment començarà
a desaparèixer. Si l'argent només està una mica
ennegrit, aquest desapareixerà en uns quants minuts. Si està
molt ennegrit necessitarem rescalfar l'aigua barrejada amb el llevat i
repetir el tractament diverses vegades per treure tot l'ennegriment. |
|
| Discussió |
| Quan l'argent s'ennegreix es combina amb el sofre per formar sulfur
d'argent; com el sulfur d'argent és negre, quan aquest es forma
sobre la superfície de l'argent ennegreix aquesta. L'argent es pot
tornar a la seva lluïssor original eliminant el sulfur d'argent de
la superfície. |
|
| Hi ha dues maneres desfer-se d'aquesta pel·lícula de
sulfur d'argent. Una consisteix a eliminar el sulfur d'argent de la superfície,
que és el que fan els líquids comercials. L'altra consisteix
a invertir la reacció i transformar el sulfur d'argent en argent
altre cop. En el primer mètode una mica d'argent és eliminada
de la superfície. En el segon en canvi no perdem cap quantitat d'argent. |
|
| El mètode utilitzat aquí no elimina argent de la peça,
ja que retorna el sulfur d'argent a argent altre cop. Molts metalls, a
més a més de l'argent, formen compostos amb el sofre. Alguns
d'ells senten una afinitat més gran pel sofre que l'argent.
L'alumini és un d'aquests metalls. En l'experiment l'alumini reacciona
amb el sulfur d'argent per formar sulfur d'alumini i alliberar l'argent.
La reacció química que representa el procés és
la següent: |
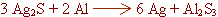
|
|
"el sulfur d'argent reacciona amb l'alumini per donar argent i
sulfur d'alumini"
|
|
| La reacció entre el sulfur d'argent i l'alumini té lloc
quan tots dos estan en contacte, mentre tots dos estan submergits en la
dissolució de llevat. La reacció és més ràpida
si l'aigua està calenta. El sulfur d'alumini s'adhereix al full
d'alumini, o pot formar petits flocs de color groc pàl·lid
al fons de l'olla. L'argent i l'alumini han d'estar en contacte perquè
un petit corrent elèctric flueix entre ells mentre la reacció
té lloc (és una reacció electroquímica, també
anomenada "redox"). Reaccions d'aquest tipus són les emprades en
les bateries dels cotxes i les piles. |
|
| (Font: La
ciència pot ser divertida) |
|
|
|
| Darrera actualització:
|
