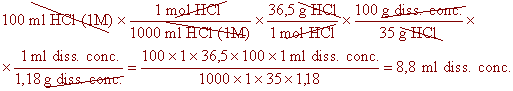| | Començar | Experiments | Galeria de Fotos | Glossari | Jocs | Pedagogia | Sortir | | |||||||||||||||

|
|||||||||||||||
| Factors de conversió | |||||||||||||||
| Els factors de conversió són essencials en la resolució dels problemes que es plantegen en química. Si se saben fer servir regles de tres poden costar d'assimilar, perquè el mateix que fa un factor de conversió ho pot fer una senzilla regla de tres... al principi. Després, conforme es van complicant els problemes, les regles de tres són del tot feixugues, mentre que els factors de conversió es transformen en simples i potents eines de càlcul, que fan possible la resolució de problemes complicats de manera més senzilla i molt més clara. | |||||||||||||||
| Què és un factor de conversió? | |||||||||||||||
| Un factor de conversió és una equivalència, un
quocient, una igualtat..., qualsevol cosa que ens relacioni dues unitats,
dues magnituds, dues substàncies, etc., que s'escriu
en forma de fracció. Podríem dir que un factor de conversió
és una fracció que val 1. Per tant, podrem escriure
el numerador i el denominador segons el que ens convingui.
Exemples:
|
|||||||||||||||
| Utilització dels factors de conversió | |||||||||||||||
| Els factors de conversió tracten els símbols corresponents a unitats, magnituds, elements químics, etc., com si fossin una variable algèbrica (una lletra: a, b, x, t, etc.), de manera que, en trobar el mateix símbol al numerador i al denominador de fraccions que es multipliquen, els podem simplificar. Així doncs, nosaltres col·loquem el factor de conversió multiplicant de la manera adient per a que el símbol que volem transformar (convertir) es simplifiqui, i que al seu lloc quedi el símbol que desitjàvem trobar. La "gràcia" dels factors de conversió és que els podem anar encadenant un darrere l'altre, i mitjançant transformacions successives, resoldre el problema proposat. | |||||||||||||||
Exemples:
a) Senzill, fàcilment resoluble amb una regla de tres (o dos): Expressa en molaritat la següent concentració: 10g de NaCl en 250 ml de dissolució, sabent que la massa molar del NaCl és de 58,5 g/mol.
|
|||||||||||||||
| Atenció: fixem-nos que simplifiquem les unitats, els nombres es queden!!! Després simplifiquem els nombres tant com ens és possible i fem les operacions que queden (en aquest cas 1000 dividit entre 25 i el resultat dividir-lo entre 58,5). | |||||||||||||||
b) difícil, necessitarem moltes regles de tres, si les sabem trobar... Quants mil·lilitres d'HCl concentrat al 35% en pes necessitem pipetejar per aconseguir 100 ml d'una dissolució 1M? Sabem que la densitat de l'HCl concentrat és de 1,18 g/ml i la massa molar de l'HCl és de 36,5 g/mol (*) |
|||||||||||||||
| En l'apartat "com es resolen els problemes de química" veurem perquè aquest problema es resol d'aquesta manera, però ara fixem-nos només en els factors de conversió: | |||||||||||||||
| 1.- Les unitats estan detallades al màxim, per evitar confondre'ns: els mil·lilitres d'HCl 1 molar (1M) no són el mateix que els mil·lilitres de dissolució concentrada (diss. conc.), és a dir, no es poden simplificar entre ells (es com si fossin dues lletres diferents, a i b). Així mateix, els grams d'HCl no són el mateix que els grams de dissolució concentrada. | |||||||||||||||
| 2.- Anem alternant la \ i la / a l'hora de simplificar, per mor d'una major claredat (què simplifiquem amb què). | |||||||||||||||
| 3.- En darrer terme fem les operacions. En aquest exemple i en l'anterior hem escrit els "1" per a que es vegi que tots els nombres "es queden", però és evident que no cal posar-los. | |||||||||||||||
| (*) Sembla molt inversemblant i un problema "fabricat" per a lluir factors de conversió? doncs el que ens demanen és agafar l'ampolla d'HCl que ve de "fàbrica" i prendre'n una quantitat per preparar una dissolució més diluïda (la de l'ampolla fumeja... és salfumant concentrat). Fixem-nos que ens hem saltat directament un dels factors de conversió: hem posat els 1000 ml HCl (1M) en lloc de posar 1 l i passar-lo a ml ..... | |||||||||||||||
| Perquè són tant útils els factors de conversió? | |||||||||||||||
| Primer. Són fàcils d'utilitzar: si el símbol que volem transformar està al numerador, només hem de posar el factor corresponent de manera que aquell símbol estigui al denominador, i viceversa. | |||||||||||||||
| Segon. Qualsevol cosa es pot fer servir com a factor de conversió: una densitat, un tant per cent, una equació... com dèiem al començament, qualsevol equivalència es pot fer servir com a factor de conversió. | |||||||||||||||
| Tercer. Fem les operacions al final: Això vol dir que podem simplificar moltes operacions abans d'agafar la calculadora (ens pot passar que multipliquem per cent i dividim per mil, llavors, simplifiquem zeros, i només ens cal dividir per deu). Per tant, en fer menys càlculs reduïm el risc d'equivorcar-nos en una operació. | |||||||||||||||
| Quart. Tenim totes les operacions a la vista: Per tant podem repassar millor i comprovar si hi ha alguna equivocació en algun factor o en alguna operació. | |||||||||||||||
|
|
|||||||||||||||
|
|
|||||||||||||||
| Darrera actualització: |