|
Problema C1.
Tot seguit presentem la informació que hem trobat
de forma resumida. Aquests paràgrafs parlen de l’hemoglobina
en i de les globines que acostumen a formar-la. A més,
trobem aspectes sobre l’evolució d’aquestes
proteïnes i com les trobem en les persones normals
i talassèmiques.
Què és l’hemoglobina?
L’hemoglobina (Hb) i la mioglobina són les
proteïnes transportadores d’oxigen als organismes
vertebrats. L’hemoglobina es troba als eritròcits
i la mioglobina, en canvi, es troba als músculs.
Tot i això, la hemoglobina va sorgir de la mioglobina
durant el curs de l’evolució, de ben segur
a partir de les nombroses mutacions que la mioglobina va
anar patint. La diferència més important
entre totes dues és que la hemoglobina s’uneix
per quatre zones diferents a l’oxigen o bé al
diòxid de carboni, mentre que la mioglobina tan
sols té un lloc d’unió amb aquestes
substàncies.
A grans trets, l’hemoglobina es tracta d’una
heteroproteïna caracteritzada pel seu color vermell
que li confereix el nucli de ferro que conté. És
formada per quatre cadenes polipeptídiques (globines)
a cada una de les quals s’uneix un grup hem o ferroprotoporfirina,
que en el seu nucli de ferro és capaç d’acoblar-se
de forma reversible a l’oxigen.
Estructures de l’hemoglobina
Estructura primària
Les hemoglobines de tots els mamífers consten de
quatre cadenes peptídiques, cada una de les quals
està acoblada a un grup hemo. Aquestes molècules
d’Hb es formen a partir de la combinació de
dues subunitats en una cadena peptídica anomenada α i
dues de β, que contenen 141 i 146 aminoàcids
respectivament.
Estructura secundària
En el cas de la hemoglobina, el contingut
de l’estructura
en hèlix-α és d’un 75%. A més
d’aquest tipus d’estructura també trobem
en aquesta heteroproteïna estructures en full
plegat.
Estructura terciària
Es tracta d’una proteïna gairebé esfèrica
(globular) amb un diàmetre de 55Å. Els grups
hem es troben en l’interior de cada una de les quatre
cadenes que formen l’Hb, en unes zones properes a
l’exterior de la molècula.
En l’estructura de l’Hb, no trobem enllaços
S-S ja que la cisteina (aminoàcid que conté sofre),
no existeix en la cadena alfa, tot i que si trobem aquest
aminoàcid en la globina beta. Tot i això,
no és possible aquest tipus d’enllaços
entre les cadenes α i β ja que tan sols les
segones són les que contenen aquest aminoàcid.
A més a més, un factor que impossibilita
encara més aquesta unió, és el fet
que dues cadenes iguals no poden mantenir un enllaç.
Estructura quaternària
La unitat funcional de l’Hb és
un tetràmer que consta de dues classes de
cadenes polipeptídiques. L’hemoglobina
està classificada dins del grup de les proteïnes
conjugades o heteroproteïnes, ja que a més
de tenir o posseir aminoàcids conté a
més a més una proporció significativa
del grup prostètic hem ja que cada cadena
del tetràmer està unida a un d’aquests
grups hemo.
Segons els tipus de globines que
es combinen, l’hemoglobina resultant podrà ser
funcionalment adequada o bé no funcionaràcorrectament
i aleshores l’individu patirà un tipus
de malaltia o bé una altra. |
Imatge
29: estructura
quaternària
de l’Hb (dibuix)
www.usaswimming.org |
Imatge 30: estructura
quaternària de l’Hb (imatge virtual
més detallada)
http://ggth.typepad.com/photos/uncategorized/betag.png
|
Com ja sabem, l’hemoglobina s’uneix
a l’oxigen. Quan la trobem unida a aquest
element, parlem de desoxihemoglobina o bé de
forma T (tensa o tirant), i és la que dóna
l’aspecte vermell intens a la sang arterial.
En canvi, quan perd l’oxigen es denomina
hemoglobina reduïda o oxihemoglobina (forma
R o relaxada), que presenta el color vermell fosc
de la sang venosa.
|
L’alfa
i la beta globina
L’hemoglobina, com hem dit, és una heteroproteïna
formada per quatre cadenes (globines) iguals dos a dos.
L’hemoglobina que trobem en un individu normal està formada
per dues globines alfa i dues de beta, i en cada una d’aquestes
quatre globines, trobem un grup prostètic, amb un
nucli de ferro que s’encarrega d’unir-se als
gasos que cal transportar. Aquest apartat, es centra en
les dues cadenes principals de la hemoglobina, alfa i beta,
tant en el seu aspecte evolutiu com genètic.
Els gens del tipus de la beta globina
(Aγ i Gγ, δ, ε i β)
dels éssers humans es troben al braç curtdel
cromosoma 11 a la regió 1, banda 5.4 (11p15.4).
Ocupen vora 60.000 parells de bases (pb), o 60 (kilobases)
de DNA. Per altra banda, en la espècie humana, trobem
dos gens de l’alfa globina. Tots dos es troben en
el braç curt del cromosoma 16 (16p13.11 a 16p13.33)
en un segment de DNA d’aproximadament 30kb.
Tots dos grups de gens no tan sols contenen únicament
la majoria de gens que són necessaris en el individu
ja adult, sinó que també expressen seqüències
que són utilitzades en diferents etapes de cada
individu. En el cas de la globina alfa, les modalitats
que trobem d’aquesta cadena són la ξ o
xi, i la mateixa cadena α, per altra banda, les modalitats
de la globina beta són la pròpia β,
la γ (Aγ i Gγ) o gamma , la δ o
delta i la ε o èpsilon. A més a més,
existeixen els pseudogens o gens que manquen de funció,
que els identifiquem amb el símbol ψ. En el
cromosoma 16 en trobem quatre de diferents relacionats
amb la globina alfa (ψα1 ψα2, ψξ, ψθ),
mentre que en el cromosoma 11 en trobem tan sols un (ψβ).
Evolució dels gens de la beta i l’alfa
globina
A les imatges-esquema següents observem l’evolució de
la beta i de l’alfa globina al llarg del temps i
mostren quines són les altres globines que s’han
derivat de cada una de les dues proteïnes principals
(alfa i beta).
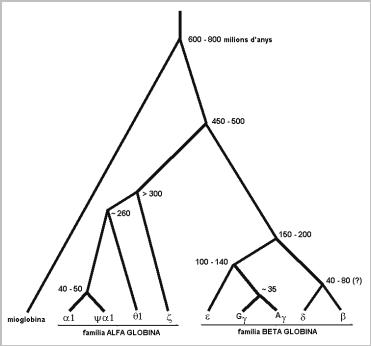 |
Imatge
31: Evolució dels
gens de la globina alfa i beta a través
del temps (milions d’anys).
www.mun.ca |
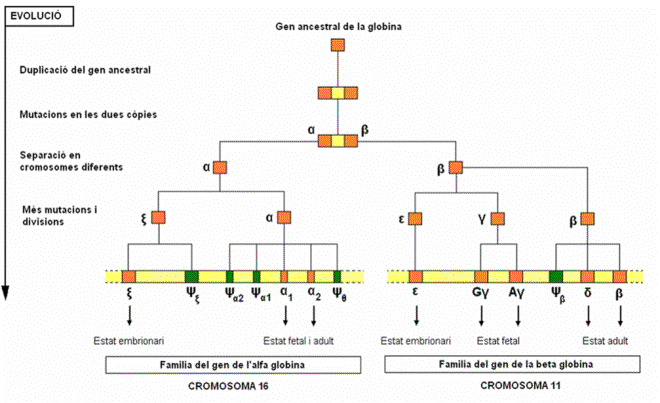
Imatge 32: Evolució dels
gens de la globina alfa i beta
Eduard Cámara Anadón
Gens i tipus d’hemoglobina
Anteriorment
hem parlat de que l’hemoglobina està formada
per dos parells de globines idèntiques dos a dos,
i que aquestes globines segons en l’estat en que
es troba l’individu (embrionari, fetal i postnatal
o adult) tenen unes característiques o bé unes
altres.
També cal dir, que hi ha casos com ara la talassèmia,
en que el curs de canvi de l’hemoglobina no sempre és
el correcte ja que aquest tipus de malaltia es caracteritza
pel fet de no sintetitzar correctament o bé completament
les globines que formen part de l’Hb, per tant aquestes
persones contindran en els seus eritròcits
un tipus de hemoglobina diferent a la que haurien
de tenir en la etapa de la vida en la que es troben.
La síntesi de l’Hb comença en les
primeres setmanes del desenvolupament embrionari i pot
ser de tres tipus diferents: les conegudes com Hb de Gower
1 i 2, i l’Hb de Portland.
A les 6 o 8 setmanes
de gestació l’expressió de
l’Hb canvia, i en aquest moment es comença
a sintetitzar únicament al fetge. Els dos tipus
de gens anomenats Aγ i Gγ apareixen en el moment
en que els gens que s’han expressat durant l’estat
embrionari desapareixen (ε i ξ). La diferència
entre totes dues cadenes és que en l’aminoàcid
136 de les seves cadenes, l’Aγ presenta una
alanina, i el Gγ presenta una glycina.
Poc després del naixement, hi ha un cavi gairebé total
de les cadenes γ per les cadenes adultes β,
tot i que no vol dir que la síntesi de les primeres
desapareixi, sinó que totes dues es formen en diferents
concentracions tant en el fetge com en la medul·la.
Ara, la que coneixíem com hemoglobina fetal (HbF)
es transforma en dos tipus de hemoglobina de l’adult,
l’HbA i l’HbA2.
Finalment, i
si l’individu no presenta cap malaltia
com ara la talassèmia o l’anèmia de
cèl·lules falciformes, la composició final
de la hemoglobina en un individu adult és aproximadament
del 97.5% d’HbA, el 2% d’HbA2 i el 0.5%
HbF, la qual cosa significa que una petita quantitat
de la hemoglobina fetal es conserva.
Fent un resum
del procés anterior, els tipus d’Hb
que coneixem són les següents:
- ESTADI EMBRIONARI
Hemoglobina de Gower 1 i Gower 2 i hemoglobina
de Portland: en l’estadi embrionari,
les cadenes ξ (xi) s’uneixen a les cadenes ε (èpsilon)
o γ (gamma).
Hb de Gower 2: (α2ε2)
Hb de Portland: (ξ2γ2)
Hemoglobina F: és la hemoglobina
normal del fetus que en la seva major part es degrada
en els primers dies de vida del nen, essent substituïda
per la hemoglobina A. Durant tota la seva vida el subjecte
normal produeix petites quantitats d’HbF. Per altra
banda, aquest tipus de hemoglobina és lleugerament
més afí a l’oxigen que no pas l’Hb
ja adulta i això permet al fetus absorbir oxigen
de forma més eficient des de l’aparell
circulatori matern.
Està formada per dues cadenes alfa i dues de
gamma (α2γ2). Més concretament, en
el lloc que ocupa la lletra gamma, s’hi poden posar
tant la globina Aγ com la Gγ, depenent de
l’individu, de forma que d’aquest tipus de
hemoglobina se’n coneixen dues versions
diferents.
- INDIVIDU ADULT
També es consideren impossibles estructures
amb un nombre imparell de monòmers de cada classe
(α3β).
La talassèmia es produeix degut a l’absència
o la reducció de la síntesi d’una cadena
de globina, la qual cosa provoca una hemoglobina inestable.
Poden ser afectades tant la globina alfa (α-talassèmia)
com la globina beta (β-talassèmia), però donat
a que la
globina alfa es troba present tant en l’Hb de l’adult com l’HbF
les alfa-talassèmies són especialment severes.
Problema C2.
Anàlisi de l’analítica
de sang
Abans de fer l’anàlisi cal saber el significat
del tots els valors o paràmetres que s’han
tingut en compte. Aquests paràmetres són:
HEMATOCRIT: % del volum que ocupen
els eritròcits sobre el volum total de sang.
VCM (Volum Corpuscular Mitjà):
la mitjana de volum que tenen els eritròcits.
Hematocrit x 10
VCM = --------------------------
Eritròcits
HCM (Hemoglobina Corpuscular Mitjana):
la mitjana de quantitat d’Hb que té cada
eritròcit.
Hemoglobina x 10
HCM = --------------------------
Eritròcits
RDW (Distribució de volum):
mesura si existeix una gran diferència de
mida entre uns eritròcits i uns altres.
CHCM (Concentració d’Hemoglobina Corpuscular Mitjana):
la mitjana de quantitat d’hemoglobina per unitat
de volum dels eritròcits.
Hemoglobina
x 100
CHCM = ------------------------------
Hematocrit
ANÀLISI
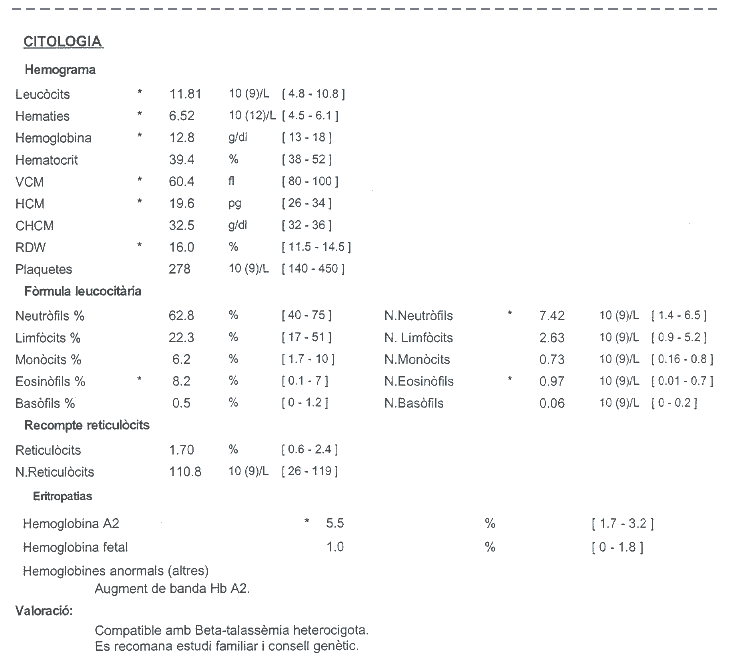
S’observa que els eritròcits es troben
lleugerament per sobre dels paràmetres màxims
determinats. Lògicament, al mateix temps que el
nombre d’eritròcits es veu alterat, també ho
haurien d’estar el nombre de reticulòcits
ja que són les formes immadures dels eritròcits,
i això no succeeix. La raó és que
en les persones talassèmiques s’acostumen
a trobar un major nombre d’eritròcits per
a contrarestar la manca d’hemoglobina i el nombre
de reticulòcits acostuma també a ser molt
elevat i en ocasions supera els valors estàndards
assignats a aquest paràmetre.
L’VCM, l’HCM i el CHCM són valors
extrets directament d’unes relacions matemàtiques
simples a partir del nombre d’eritròcits,
l’hemoglobina i de l’hematocrit. Tot seguit
analitzarem aquests tres paràmetres individualment:
VCM: els valors en aquesta persona de Volum Corpuscular
Mitjà estan per sota dels valors normals. Això s’explica
degut a que els eritròcits de les persones talassèmiques
són microcítics, és a dir, són
més petits. Per tant si els eritròcits
són més petits, el volum corpuscular mitjà estarà per
sota del normal. Com podem veure, que el nombre d’eritròcits
es trobi per sobre dels valors normals no influeix en
l’VCM i a més reafirma que les persones
talassèmiques tenenuns glòbuls vermells
més petits del normal.
HCM: si els eritròcits són més
petits és perquè l’hemoglobina que
contenen no està sintetitzada correctament. Per
aquesta raó, el valor que trobem sobre l’Hemoglobina
Corpuscular Mitjana és inferior al que està estipulat
pels paràmetres que ens marquen.
CHCM: el valor que s’observa es troba molt a prop
del mínim que ens marquen els paràmetres.
La Concentració d’Hemoglobina Corpuscular
Mitjana ens senyala la proporció entre la quantitat
d’hemoglobina i el volum en total del glòbul
vermell. La CHCM d’aquesta persona, tot i ser talassèmica,
es troba dins dels paràmetres de normalitat ja
que tot i que el volum dels eritròcits és
més reduït, també ho és la
quantitat d’hemoglobina.
RDW: és un paràmetre que ens diu si hi
ha molta diferència entre el volum dels diferents
eritròcits. En aquesta analítica veiem
que el valor que s’obté es troba per sobre
del màxim que ens marquen els paràmetres,
la qual cosa ens diu que hi ha força diferència
entre les mides dels diferents eritròcits, i per
tant que hi ha glòbuls vermells que han estat
sintetitzats correctament i n’hi ha que no.
En referència a la fòrmula leucocitària,
de les mateixes cèl·lules tenim dos
valors diferents separats en dues columnes. La diferència
entre totes dues columnes és que la de l’esquerra
ens dóna el resultat en tant per cent, i la
de la dreta ens dóna el resultat en valor
absolut. Hi ha casos, com el dels neutròfils
en aquest anàlisi, en què hi ha variacions
entre una columna i l’altra. Per altra banda
els eosinòfils
també estan alterats tot i que no ho fan d’una
manera prou significativa. Per a detectar alguna
anomalia mitjançant l’alteració cal
que aquests valors siguin molt elevats, i ens indiquen
que s’està patint
una al·lèrgia, una parasitòsi,
o altres síndromes més poc comuns com
ara el de Hodking. Aquests dos casos relacionats
amb els leucòcits, que en l’apartat
de la fòrmula
leucocitaria surten alterats, no tenen res a veure
amb ser talassèmic o no, i depenen de la situació immunitaria
de cada persona.
Per últim, si ens fixem en l’apartat de
les Eritropatíes, observem que l’Hemoglobina
A2, formada per dues cadenes alfa i dues de delta, es
troba molt per sobre dels paràmetres marcats.
Això és el que ens acaba de rebel·lar
que la persona que estudiem és beta talassèmica
minor, ja que com no pot sintetitzar del tot correctament
l’hemoglobina A (dues cadenes alfa i dues de beta),
substitueix aquesta hemoglobina per l’Hb A2.
Resultats de les equacions
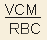
RBC: és el recompte d’eritròcits
en milions.


|